尖端医疗的真相 The Bleeding Edge(2018)

又名: 流血的边缘 / 前沿医疗:福音还是风险? / 尖端医疗的真相,你安全吗?
导演: 科比·迪克
主演: Robert Bridges Angie Firmalino Rita Redberg Stephen Tower
类型: 纪录片
上映日期: 2018-04-21(翠贝卡电影节) 2018-07-27(新加坡)
片长: 99分钟 IMDb: tt8106576 豆瓣评分:9.1 下载地址:迅雷下载
简介:
- Netflix原创纪录片,讨论美国利益导向,且价值高达数十亿美元的医疗器材产业,如何将风险天天加诸在病患身上。
演员:
影评:
美国有种永久节育器Essure,像一根螺旋针一样,被植入女性输卵管,最后效果是输卵管会因为这根金属针而作出反应,最后阻断输卵管通路,起到节育作用。
被植入十余年后的部分女性,出现了腰酸,腿酸,全身无力,子宫刺痛的现象;这些出现这种现象的女人,部分在针取出来后,仍然有更加严重的症状出现,子宫大流血,不能有性生活,还有部分不能取出来,变成无数的金属片散落在子宫,部分人需要切除子宫。
另一个产品叫疝气补片,是一种特殊材质的网,少数女性在分娩后体内相关组织松弛,会出现尿失禁现状,这种网状用于永久植入体内,起到支撑相关组织的作用。然而,植入这些金属网的女性,同样出现大量的问题,无力,连爬楼都爬不了,发烧等等,这种网几年后跟组织与肉融合在一起,因为持续收缩,不断地在挤压体内的组织和骨头,影响了器官功能。当病人想取出来的时候,事实上相当难取,几年做了十七八次手术,仍然无法完全取出。当性交时,金属网割伤了病人丈夫的器官,性生活以后基本上不可能了。
有一种叫达芬奇的机械臂手术仪器,医生用这种机械手术仪器为几个女性做了子宫切除手术,谁知,做了这些手术的女性,体内的肠竟然在走路和上厕所时,从阴道口掉出来!这与对操作这种机械臂的医生缺乏培训有关,有医生反映需要300次完整的手术才能基本上算是熟练,而卖这个器材的公司intutive surgical在卖出这个产品给医院以后根本就没有给医院太多培训,导致医生做用这个机械臂做手术时出现问题。
有个人换了髋关节,用了金属钴,结果钴元素扩散至全身,导致他的神经系统出现错乱。
假隆胸能引发一种罕见的癌症。
用于粉碎纤维瘤以更好取出的器械,竟然导致癌细胞在全身扩散.
。。。。
看了不禁倒抽一口凉气,片中所有的受害者一生都毁了。
那么是什么原因酿成这些恶果呢?
FDA监管疏漏
医疗器械上市不像药品上市这么严格,药品上市需要经过创新药或者是仿制药申请,其中还包括临床实验或生物等效性实验,申请流程十分严格,耗费以亿来计,时间上以十年来计,保证了药品的安全性和有效性。但是医疗器械,尤其是那种植入型的,由于其副作用可能需要经年累月才出现,而当下主要是以病人植入后一两年之间作为观察,且因为这样的病人数量甚少,没有药品所有的三期临床实验这种严格的流程,只需要证明拥有所对标的业已上市的器械的功能即可,通常也只会给FDA呈现一到两个病人的证词。事实上,有些可能连证词都不用。
医疗器械公司为追求利润欺上瞒下
比如疝气网,就算是内部研发成员提出安全性风险,就算是用在实验病人身上出现的不良反应,就算是已经上市后出现的医疗事故,公司都会采取掩饰手段,一方面以期FDA不会成为上市的阻碍,另一方面哄骗医生和病人尽快使用,信誓旦旦。对于已经售卖出现的器械,因为已经实现了利润,在培训方面又可省则省。
医生追求高利润,会尽量上马新器械。
吃回扣这种事情且不说,新的器械因为所宣传的技术含量与相对于旧技术的优点,定价也更高,医生在追求更高利润,以及更稳妥上面,一般会选择前者。他们会宣传新器械的好处,鼓励病人使用。
FDA和医生原本是应该跟病人一道,对抗医疗器械公司,但现实是,医生事实上是利益的一个大极,比之于跟病人一起作战,他自己的利益诉求是显著的;而FDA却已经跟医疗器械公司站在了一起,FDA有相当多已退下来的官员,通过旋转门去了医疗公司当顾问,为医疗器械公司更快地拿 到上市批文做贡献;而FDA的官员,也同样来源于医疗行业。FDA有了更多的来自医药公司、医疗器械公司的利益。在这里,病人是唯一被放弃的,孤独的一群。
我这些天在做医疗产业相关研究,为医疗行业各种发明感到震撼,觉得人类健康前途很光明,这部片给了我重重一棒,让我清醒了不少。新技术、突破性技术是层出不穷,然而,因为监管器械并没有监管药物来得严格,这些器械的隐患与风险是相当大的,一句话:它远没有说得那么好!一定要记住,你的身体属于你,所有的风险都是你在承受,医生并不能够帮助做决定,有时他追求自己的利益已经超过了你自己的利益。面对医疗器械,一定要多调研其风险,对于植入性器械,可不做的情况下尽量不做。
我想起一个初中同学,他的眼睛1000度以上,后面做了激光手术,就不用戴眼镜了,但是他读博后又开始戴眼镜了,后面我问他,他说眼睛比以前更差了。
我最近想换个眼镜,也经历了在医院做验光时,觉得医生不可靠的事。整个过程是这样的,我在医院(还是个三甲医院)和五家眼镜店都做了验光,为什么我要在六家机构做简单的验光待会再说,在眼镜店直接付给他们钱,要求只做验光。他们做得很仔细,并且都是器械加人工,很认真。而在医院,感觉医生真是有点敷衍,因为临近下班,但还没到下班点,他一直说他儿子乘飞机回国,想要快点搞完我这个验光好去接他,最后验出的度数,医生验的度数次高,除了一家,其余眼镜店的都没那么高,其中有一家还给了建议,说虽然测得这个度数,但实际配镜可以再下调一些度数,这样不会产生头晕等现象。说实在的,我很难判断到底是医生验得对还是眼镜店验得对,也正因为医院与眼镜店,以及眼镜店彼此之间都有差异,我就多找了几家眼镜店验,毕竟眼镜一带就会带五六年,做细致一点也对未来也是好的。联想起医生在整个过程三番四次跟我提香港的一种验光技术,因为我每一次都没接他这个话题,他在整个验光过程中时不时“不经意”地提到,我回忆的时候越发觉这之间可能有猫腻,对他的信任又降低了,所以最终选择了一家我最信任的,同时佩戴相应度数觉得最舒服的一家。
通过我个人接触的两个案例,只想说明两个道理:改变原有机体的医疗器械都是有风险的,以及,医生并不是都是全心全意站在你这边的。
先把纪录片结尾的建议放上来:
- 调查已经在自己体内或者将要被植入自己体内的设备是否安全,新产品不代表好
- 昂贵或者高风险的手术一定要多听取各方意见
- 询问你的医生他做过多少台手术
- 在医院的时候要有家人或朋友的陪伴,让他们为你发声
- 可以上网查你的医生是否被医药公司赞助
从此以后,再也不敢相信医疗器械行业了
2018年,无论对于中国和世界,还是对于我自己,无疑都是不停地挑战我对于医疗行业认识的一年。
从疫苗事件到,《我不是药神》,从家人突然重病,到今天看了一半就已经不寒而栗的纪录片Bleeding Edge。
我的确不该在午饭的时候看这么沉重的纪录片的。
从保证可以永久避孕,无副作用的Essure到特别适合运动的人使用的髋关节假体到声称安全创新的附着在女性体内的强生网片。
结果,没有一样是真正安全的。
每一样医疗器械背后都有大量的受害者。
我去FB搜索Essure,看见现在Essure Problems小组人数已经多达3.9万人,她们在7.27 Bleeding Edge上映时,还举行了观影派对。
然而,今天等来的却是来自拜耳公司无情的否认。
下图:拜耳7.27发布的声明,坚持不改变对于Essure产品对于人体健康无害的观点
这部纪录片让我再次感受到画面的冲击力,那是比文字强烈一百倍的。
当我看到副作用为“全身疼痛、手脚不自觉颤抖、下体出血、记忆衰退”等描述时,我可能并不会觉得有些什么。
但是,当我看到画面,听到那些曾经也是有幸福家庭、健康乐观的人们,如今坐在镜头前面倾诉自己的故事,还时不时笑一下,似乎是在自嘲时,我的心就像是被狠狠地拧了一下。
看的时候忍不住腿软发颤,倒不是由于片中出现的血腥的画面,因为那可能是正常的手术都会有的。反而是那些受害者的描述,看似轻描淡写地诉说着几年来摆脱不掉的,也许会伴随一生的生理心理上的折磨。这个时候,我会尤其难受。
Essure
看到Essure受害者们自发成立FB小组,然后逐渐壮大,到处搜集资料和证据,筹集900美元资金购买当时FDA审批Essure的视频,去美国最大的妇科医疗大会抗议,一起去国会寻求帮助,觉得她们好艰难,但是也好坚强。
可是,这些应该由她们承担吗?
 Essure本体
Essure本体 Essure FB小组
Essure FB小组强生的网片

还有因为分娩导致控制不住泌尿所以被建议植入强生生产的网片(mesh),可是导致一系列并发症,但是又因为网片和器官已经裹在一起,根本无法全部取出,导致后续更多的手术。
而且,因为网片放置在阴道,所以残存的网片还会在丈夫插入的时候割破阴茎,导致女性根本不能回归性生活,可能是永远地失去了和爱的人亲密的机会。
有许多女性因此婚姻破裂,丈夫离开自己。
还有的因为经常的疼痛而无法工作,只好带着孩子流离失所。
这些医疗器械,一旦植入,可能很难取出,或者至少完整无损的取出。而且,取出之后还可能会产生更多的并发症,然后一个接一个的手术做下去。
纪录片中提到的还有隆胸假体、震颤器、以及各种设备出问题。
也包括CT扫描仪中含有的辐射会导致某些人患癌症,但是近年来CT的使用却是原来的4倍。
据统计,每年有5万美国人因CT扫描剂量过度而患癌症。
纪录片中令我记忆很深刻的还有那位有四个女儿的拉美裔妈妈。她在植入Essure之后就离婚了,因为身体不断需要手术,丈夫离开了她。
最令人气愤的是,这位母亲在发现自己下体出血异常去就医时,却遇到了种族歧视。
上学期在爱丁堡人类学课上读到关于black hardiness的刻板印象建构以及各种在医学界流传的种族歧视,即认为黑人女性的身体更加能够忍受疼痛,因此会让她们做更疼的手术,也少给她们很多本应得到的药。同样受到种族刻板印象的还有拉美裔。
这位母亲植入在Essure之后,经常下体出血,结果医生却说,可能因为你是拉美裔吧。
我记得她复述的时候,就笑了。
“我从小就是拉美裔,可是以前也从来不会有这种情况啊。”
这种physician racism叠加在本来就已经十分悲惨的案例上,显得更加魔幻现实了。
纪录片中问了许多问题,也是我们需要问的:
为何一个医疗产品要陪伴人的一生,可是它的临床试验研究窗口只有12-18个月?
为什么医学研究现在大多是行业资助,而不是政府?
为什么FDA的存在好像形同虚设,受害者的声音根本没有得到倾听和重视?
当人们采访到当年参与临床试验的女性时,才发现她们的意见根本没有得到倾听,甚至公司公然修改她们的答案。
医药公司:你对产品还满意吗?
受试女性:不满意
医药公司:但你没怀孕吧?
受试女性:是的
医药公司:那就是有效,你肯定满意
而且,他们还会修改受试者的答案。本来受试者报告有疼痛,他们会划掉,变成没有疼痛。
哦,最令人震惊的是,Essure声称避孕成功率高达99%以上,可是实际数据显示,使用Essure的女性是结扎女性怀孕率的7倍。FB上甚至成立了E-babies小组,而这些宝宝们出生后的健康状况也十分堪忧,还有不少早产甚至夭折。
下面几个现实更加令人心寒:
- 从前,政府提供资金进行临床试验,但是在过去的20年里,70%的生物医学研究都是行业资助
- FDA的医生和科学家意识到了问题,但是当上报到缺乏医疗管理经验的上级时,却遭到了打击报复,安装监视软件spector(两秒钟截屏和键盘按键)
- 由医疗公司派出的游说团体很厉害,专门针对政客游说以降低医疗器械行业的评判标准,从而使得自己的产品可以很轻易就上市
- FDA的很多高层领导都和医疗公司有直接利益关系,许多甚至离职之后直接去医疗公司工作了
我不知道还能说些什么了,只是希望更多人去看一看这部纪录片,意识到问题的严重性吧。
可能就像片尾她们在国会的时候被告知,虽然国会会从内部推动立法,但是,真正的改变还是来自外部的压力,要靠你们的团结去施加压力。
所以,可能越多人知道,改变现实的可能性就越大一些吧。
该片给我很大的震撼,因为一次避孕手术而毁了整个生活太让人心有戚戚,肠子流出下体也是我作为一个女生万不敢去想的可怕画面。
但即使作为一个学术垃圾,也会在同情片中受害者的同时觉察到片中很多观点似乎具有太明显的倾向性,“给我你的参考文献和数据”。作为记录片光靠讲故事是很难说服人的。
同时我们也知道,生活中没有百分之百的事情,更别说在医学领域中,即使打个喷嚏也有丧命的可能,而医学的发展却不能因噎废食,要看研究者是否有足够的投入和人道主义精神,要看政府机构时候有进行严格周全的审查,要看厂家是否对医生进行了详尽有效的培训,要看医生是否将必须的治疗步骤准确实行,是否将可能的风险明确告知,要看风险出现后社会的保障机制。这个体系是非常庞大而复杂的。这部片子给我的感觉,他的论调是“这些厂家只是为了敛财而不断推出新的医疗器械,在明知其严重危害的情况下还将其投入市场,而那些FDA的审查人员也是敷衍了事,他们和医疗公司沆瀣一气,利用职位便利相互输送利益,都是狼心狗肺的东西”。
现实生活中可能确实存在这种阴暗事实,但如此强烈的指控倾向让我在最初的震撼之后感到有些不适,这不是一个足够客观的纪录片。你可以说“在这些人身上,我们发现,在一件创新器械的研发和使用过程中仍然存在诸多问题,研发到使用需要大量的临床实验来发现可能提前无法预知的问题,审查方式尚且有所欠缺,厂家对医生的培训不够,医生在手术的操作中可能出现问题,这些风险即使被提前告知,但对于个体来说,0.1%的风险落在一个人身上就是100%,我们表达对这种情况的悲悯,呼吁医疗公司和政府监管更加严肃的承担起他们的责任。”
去找了拜耳的回应,以下是我顺手做的翻译练习,括号内加粗语句是我自己的想法,仅帮助自己理解,所有内容与拜耳无关,原文会贴在本文最后,请感兴趣的大家对照阅读。
翻译文本:
拜耳关于Netflix《The Bleeding Edge》的情况说明书
WHIPPANY, N.J., July 27, 2018 /PRNewswire/
拜耳今日发布了关于《The Bleeding Edge》的情况说明书,这部纪录片于7月27日在Netflix首映,有大量内容涉及到了Essure。Essure曾是FDA批准的唯一一种无创的永久避孕形式,而现在却成了纽约时报、CBS新闻及其他媒体的报道主题。该情况说明书基于拜耳对该片在2018年4月21日Tribeca电影节版本的评论,意在鼓励大家对于Essure进行基于科学的讨论。拜耳提醒已植入Essure的女性,该设备仍然安全有效,从未改变。
作为女性健康领域的领导者,拜耳坚信广大女性和他们的医生制定生育健康决策都应该基于可靠的科学支持。但是相反,《The Bleeding Edge》中的Esuure形象非常缺乏科学支持,即使拜耳在影片完成前就向制片方提供了大量关于Essure的科学信息。该影片大量基于个人故事和有选择性的信息来呈现提前预设出来的Essure形象,而完全无视了那些可以支持FDA做出的“Essure的益处大于其风险”决议的科学证据,和该设备的警告声明。同时,该影片还大量依赖于很多矛盾的信息源,而隐藏了他们潜在的偏向性。这对于有赖于Essure来保障其生殖健康的广大女性来说是一种伤害,这可能会鼓励她们去移除该设备,这样她们就要承担风险和不必要的手术伤害。(拜耳曾向制片方提供相关科学证明但并未被提及;片中也并未提及拜耳对于该产品提出的警告声明;这种言之凿凿的引导会让其他正常使用的女性试图通过手术移除设备,从而可能带来不必要的痛苦和其他风险)
值得注意的是,关于Essure,该片的唯一科学数据来源于发表在JAMA杂志的“the 2018 Bouillon study”,而片中展示的部分其实是该片的制片方脱离了上下文的断章取义。纵观全文,该研究其实恰恰驳斥了该片所树立的Essure形象。该第三方研究对比了植入Essure的女性和接受了输卵管结扎的女性,他们发现,不论是术后一年还是术后三年,所有影片中提到的Essure带来疼痛和子宫切除,其实在使用Essure的女性身上出现的概率要低于输卵管结扎的女性。该研究的作者总结道:“这些发现并不支持与宫腔镜手术相关的方法(例如Essure)会带来医疗风险提高。”制片方对于该重要结论绝口不提,显然是因为这与他们预设的观点相矛盾,这确实会引起大家对于该片客观性和准确性的怀疑。(该片援引相关研究却断章取义,对与自身设定相反的研究结论避而不谈)
而Essure相关的科学证据总共包含了40篇已发表论文,包括对200000名女性长达20年的跟进,并且证明了Essure的安全性和有效性,而这些在影片中并未提及。而且FDA也没有改变他们关于“Essure的益处大于其潜在风险”的结论。(Essure的有效性基于大量的研究报道)
该片对于Essure的大部分观点都是基于对该设备有所担忧的女性的故事,而并非科学讨论。拜耳对任何有关其药品或设备的关心都十分重视。并且,值得注意的是,该片有没涉及到任何一位对Essure满意的女性。这个省略很重要,因为在为期3,6,12,18,24,36,48和60个月二期实验和关键性临床试验的随访中,将配有Essure的舒适度评级为“良好”或“优秀”的女性不低于99%。而在临床实验中,五年后反馈体验在“及格”到“非常满意”区间内的女性高于97%。该数据总结在FDA在the 2015 Advisory Committee会前的执行摘要中。
任何关于该片和Essure的讨论都不能避开“移除”问题,这也正是该片中多数女性讨论的重点。该片对于这一关键点并没有给以足够的重视。向广大女性传播关于Essure的不准确甚至误导性的信息,或是鼓励她们通过摘除子宫来移除该设备,是一种潜在的重大公共安全事件,因为这会误导那些配有Essure的女性想办法移除它,这是不必要的,反而会导致新的,额外的健康问题。更重要的是,引起关注的子宫切除术其实与Essure的使用说明并不相符,使用说明中提到“Essure的移除一般不需要进行子宫切除”,并在说明书中给出了其他方法。该使用说明是基于科学/临床数据和全球医学专家的意见制定的。拜耳强烈建议配有Essure的女性,如果有任何问题和担忧请咨询专业的内科医生。(片中很多女性采用子宫切除来移除设备,这不是使用说明推荐的方法)
《The Bleeding Edge》还有赖于一些人来解释和证实他们关于Essure的故事,而该片其实隐藏了一些矛盾之处,这对于观众评价这些人和该片的可行度来说至关重要。例如,心理学家Diana Zuckerman在本片出境,她在批评Essure的论坛中十分著名。她在the 2015 FDA Advisory Committee会议中反对Essure,并在同年参加了由批评Essure的宣传组组织的另一场会议。并且她作为付费专家参加了至少一起针对Essure的诉讼,这是纽约时报在2018年7月20确定的内容,而在本片中并未提及。
同样的,Madris Tomes在本片中作为独立专家出现,但其实她也有很长一段时间和反Essure小组一起工作,并且在今年二月的会议上加入了他们。2016年5月9日,由律师事务所Unglesby + Williams公布的一则有关Essure的新闻称她受Unglesby + Williams雇佣。这件反对Essure的工作并未在本片中提及。
本片还采访了Dr. Julio Novoa,但是观众并不知道的是,他一直很激进的推荐女性采取手术方法移除Essure,并且他在其中还有经济利益。此外,Dr. Julio Novoa并不是受到职业认证的妇产科医师,并且从未接受过Essure相关的产品培训。(以上列举了三位出境专家,说明他们一直以来都有反对Essure的倾向,而且都在这种反对中有不同形式的获利,这个Dr. Julio Novoa并不是受到职业认证的妇产科医师,并且从未接受过Essure相关的产品培训我真是惊呆。)
本片还略去了任何关于已获FDA批准的使用说明的内容。该使用说明向医生提供了关于该产品的重要信息,并包含了Essure可能导致的潜在风险的细节。例如,使用说明超过20次提及到了潜在的穿孔风险,还包括很多关于疼痛、过敏和超敏反应,这些都是基于Essure的科学数据。(拜耳在使用说明中明确列举了该设备的潜在风险,并要求医生向患者说明)
该片的其他内容也并不真实,只是为了让Essure显得不安全或/和无效。例子之一就是对Essure的2002 FDA Advisory Committee meeting部分的误导性和选择性的剪辑。该片称委员会成员拿严重不良事件的可能性开玩笑。他们其实没有做这样的事情。咨询委员会在那一部分甚至并没有提及不良事件或是Essure的安全性。所有的科学证据,临床试验和超过20年的科学和临床经验都依然支持Essure的益处大于其风险,并且在依赖Essure进行避孕的病人中,其有效率达到了99.3%。(片中最令人对FDA审查制度胆寒的开会片段真实性存疑)
Essure是一种创新型的三级医疗器械,经过了FDA的RMA审查,这也是该机构对医疗器械最严格的审查方式。自Essure在2002年投入使用以来,该机构还在原有基础上对Essure进行了48项补充审批并认证了其安全性。
在2018年7月20日,拜耳宣布其决定自2018年12月31日起自愿停止Essure作为永久避孕方案在美国的销售和推广。这项决定基于近年Essure在美国销售额的下降和Essure业务不可持续的结论。造成Essure在美销量下滑的因素有很多,包括永久避孕法的使用率下降,而其他避孕方法例如长效可逆的避孕法的增加,以及对该设备不准确和误导性的宣传(例如The Bleeding Edge)等。重要的是,Essure的利弊性是没有改变的,而且拜耳坚持认可该产品的安全性和有效性。(Essure退出市场不是安全问题,而是因为其他避孕方法更受欢迎,或是类似本片的负面宣传对公众的误导导致销量不佳)
关于Essure
Essure通过造成输卵管堵塞来帮助女性实现永久避孕(女性绝育)
重要安全信息
警告:一些采用Essure进行永久避孕的病人经历了一些不良事件,包括子宫和/或输卵管穿孔,植入物进入腹腔或盆腔,持续疼痛,以及疑似过敏或超敏反应。如果需要移除设备来解决这些不良事件,则需要进行手术。这些信息应该在讨论Essure的益处和风险时向有意采用该设备的病人说明。
Essure不适用与以下情况:不确定是否要永久绝育,疑似怀孕,只能植入一支Essure,已经结扎,已知对显影剂过敏,不愿意进行Essure确认测试,有不明阴道出血,或是女性生殖器官疑似或已知患有癌症。
以下情况则应暂缓植入Essure:过去6周内已经怀孕,患有妇科感染,或是正处于经期后半期。
以下情况应向医生说明:正在服用免疫抑制剂药物,确认或可能对金属、聚酯纤维、镍、钛、铂、银-锡或不锈钢等Essure成分过敏,正在使用IUD进行避孕,过去做过或未来考虑通过子宫内膜切除来减少子宫出血。
警告:请在进行Essure植入前确定您已经生过孩子,因为Essure是一种永久性的绝育方案。
警告:你需要同时采用其他方法来避孕,直到通过Essure确认测试(手术3个月后),并且你的医生明确告诉你可以完全依赖Essure来避孕。对一些女性来说,Essure生效时间可能大于3个月,需要在6个月时重新进行确认。和你的医生讨论在这段时间你应该采用什么方式避孕。如果你在受到确认之前就完全依赖Essure进行避孕,那你会有怀孕的风险。
在手术中:在市场前调研中,部分女性(9.3%)经历了轻度到中度的疼痛。你的医生可能不能正确的进行植入。在少数病例中,Essure在植入中可能会发生部分破碎。如果发生破碎,在适当情况下,你的医生会移除这些碎片。在使用子宫镜、Essure或其他器械时,有可能造成子宫或输卵管穿孔。在市场前调研中,Essure植入造成的穿孔发生率为1.8%。穿孔可能会导致肠道或膀胱出血或受伤,可能会需要手术治疗。你的医生可能会建议采用局部麻醉。向你的医生咨询这种麻醉的风险。
术后:一些女性经历了轻度到中度疼痛(12.9%)和/或痉挛(29.6%),阴道出血(6.8%),及盆腔或背部不适。一些女性出现了头痛,恶心和/或呕吐(10.8%),头晕和/或晕倒。在术后应该安排人照顾你。在极少数病例中,Essure可能会被排出体外。
在Essure确认测试中:测试需要照X光,你可能会暴露在低剂量的辐射中,大部分是X射线。一些女性会出现恶心和/或呕吐,头晕和/或晕倒,痉挛,疼痛或不适。在极少数病例中,有些女性可能会留疤或感染。
长期风险:在Essure植入后可能会出现不同程度及持续时间的疼痛(急性或持续性),更有可能出现在有疼痛史的女性身上。也有病例中出现Essure被植入到腹腔和盆腔下部。若出现这种情况,你将不能依赖Essure进行避孕。对该设备成分过敏的病人可能会经历过敏反应。此外,一些病人可能会在术后出现对镍或其他设备成分的过敏反应。过敏反应的症状可能包括荨麻疹,皮疹,肿胀和瘙痒。尚无有效的测试来语言谁会对该植入发生反应。没有哪种避孕方法是100%有效的。Essure植入后也可能会发生宫外孕。这会危及生命。如果需要移除植入物,则需要进行手术。
Essure的安全性和有效性尚未在21岁以下或45岁以上的妇女中确立。
Essure不能预防艾滋病毒或其他性传播疾病。
仅限处方。
重要信息
注意:联邦法律限制这种设备只能在医生的指导下销售;仅供具备子宫镜知识的医生使用;阅读并理解使用说明书和医师培训手册;并成功完成Essure培训项目,包括指导实习直至能力建立,通常为5例。
本设备的销售和分发仅限于用户和/或以拜耳提供的批准标签中规定的形式和方式向患者提供有关本设备的风险和益处的信息的用户和机构。
和你的医生谈谈Essure并讨论它是否适合你。在决定进行Essure手术之前,与医生一起检查患者信息手册中的患者-医生讨论清单。
拜耳是一家全球性的企业,在医疗保健和农业生命科学领域拥有核心竞争力。其产品和服务旨在造福人民,提高人民的生活质量。与此同时,集团的目标是通过创新、增长和高盈利能力来创造价值。拜耳致力于可持续发展的原则,以及作为企业公民的社会和道德责任。2017财年,集团员工约99800人,销售额为350亿欧元。资本支出达24亿欧元,研发支出达45亿欧元。更多信息,请访问。
拜耳原文:
Bayer United States of America
Bayer Fact Checks Netflix's The Bleeding Edge
WHIPPANY, N.J., July 27, 2018 /PRNewswire/ -- Bayer today released a Fact Check of The Bleeding Edge, which premieres on Netflix on July 27, devotes significant time to Essure, the only FDA-approved non-incisional form of permanent birth control, and is now the subject of media coverage by The New York Times, CBS News, and others. This Fact Check is based on Bayer's review of the film's premiere at the Tribeca Film Festival on April 21, 2018 and is intended to encourage a science-based conversation about Essure. Bayer also is reminding women with Essure that the safety profile of the device remains positive and unchanged.
(PRNewsfoto/Bayer)
As a leader in women's healthcare, Bayer believes strongly that women and their physicians should make reproductive health decisions based on sound science. In contrast, the portrayal of Essure in The Bleeding Edge lacks scientific support, despite the fact that Bayer provided the producers with extensive scientific information on Essure before the completion of the film. The film presents an inaccurate and misleading picture of Essure by relying almost entirely on anecdotes, cherry-picking information to fit a predetermined conclusion, ignoring the full body of scientific evidence that supports the Food and Drug Administration's (FDA) determination that Essure's benefits outweigh its risks and disregarding the appropriate warnings that accompany the device. The film also relies on many conflicted sources without disclosing their potential biases. This does a disservice to the thousands of women who rely on Essure for their reproductive health, as it may encourage them to pursue risky and unnecessary surgery to remove the device.
Notably, the film's only reference to scientific data regarding Essure is the 2018 Bouillon study published in the Journal of the American Medical Association ("JAMA"), which its producers cite out of context and portray in its least favorable light. Taken as a whole, the study actually undermines the central premise of the film's representation of Essure. The independently funded research compared women with Essure to those who had tubal ligation surgery, the only other method of permanent birth control, and found that many of the concerns described in the film with regard to Essure -- pain (analgesic use) and hysterectomy -- were lower in Essure patients than in tubal ligation patients at both one and three years post procedure. The authors of the study concluded: "These findings do not support increased medical risks associated with hysteroscopic sterilization [e.g., Essure]." The decision by the filmmakers to exclude highly relevant conclusions from a study they cited, apparently because they conflict with their desired narrative, do raise serious concerns about the objectivity and accuracy of the movie.
The totality of scientific evidence, which was not discussed in the film, includes 40 published studies involving approximately 200,000 women over two decades, and demonstrates the safety and efficacy of Essure, which has remained consistent over time. The FDA also has not changed its conclusion that Essure's benefits outweigh any potential risks.
Most of the movie's focus on Essure is told not through science, but rather through the stories of women who reported concerns about the device. Bayer takes any concerns regarding its medicines and devices seriously. Still, it is notable that not a single woman who is satisfied with Essure is included in the film. This omission is important because in the Phase II and Pivotal trials at follow up time points of three, six, 12, 18, 24, 36, 48, and 60 months, at least 99% of women were reported to have rated comfort of wearing the Essure inserts as "good" or "excellent." In the Pivotal trial, at least 97% of women were reported to be "somewhat" to "very satisfied" at all visits through five years. This is summarized in FDA's executive summary prepared in advance of the 2015 Advisory Committee.
No discussion of the movie and Essure should ignore the issue of removal, which most women featured in the film discuss. The film provides no balance on this important topic. Providing women with inaccurate or misleading information about the safety of Essure, or encouraging removal via hysterectomy, is potentially a serious public health issue as it may lead women with Essure to unnecessarily seek removal, and can result in new or additional health problems. Moreover, the singular focus on hysterectomy is inconsistent with Essure's FDA-approved Instructions for Use (IFU), which state that "hysterectomy generally is not required to remove the Essure inserts" as there are other methods identified in the IFU. The IFU is based on scientific/clinical data and opinions from medical experts worldwide. Bayer strongly encourages women with Essure who have questions or concerns to consult with their physicians.
The Bleeding Edge also relies on a number of sources to explain and validate its story regarding Essure, but the movie does not disclose conflicts that are essential for viewers to fully evaluate the credibility of these individuals and the film. For instance, psychologist Diana Zuckerman appeared in the film and is well known in the Essure critics community. She spoke at the 2015 FDA Advisory Committee meeting arguing against Essure and participated in another meeting that same year with the FDA organized by an advocacy group that has been critical of Essure. She has also served as a paid expert in litigation for at least one Essure plaintiff, a fact confirmed by The New York Times on July 20, 2018, but not disclosed in the film.
Similarly, Madris Tomes is presented as an independent expert in the film, but she also has a long history working with an anti-Essure advocacy group and joined them in congressional meetings in February of this year. A May 9, 2016, press release by a plaintiff law firm involved in the Essure litigation, Unglesby + Williams, reported on Tomes' work on Essure and described her as someone who was "hired by Unglesby + Williams." Again, this litigation-related work against Essure is not disclosed in the film.
Dr. Julio Novoa was also interviewed in the film, but viewers were not told that he aggressively markets surgery to women to remove Essure and has a financial interest in recommending removal of the product. Dr. Novoa is not a board-certified OB-GYN and has never been trained on the Essure procedure.
The film also omits any mention of the FDA-approved Instructions For Use (IFU), which provide doctors with important information about the product and include detailed references to the potential risks for Essure. For example, the IFU mentions the potential risk of perforation more than 20 times, contains multiple references to pain and allergic or hypersensitivity reactions – all based on Essure data.
Other content in the film is completely misrepresented in order to make Essure appear unsafe, ineffective or both. One example is the inclusion of a misleading and selectively edited portion of the Essure 2002 FDA Advisory Committee meeting, which recommended the approval of the device. The movie suggests that members of the committee joked about the possibility of serious adverse events. They did no such thing. The Advisory Committee was not even discussing adverse events or the safety of Essure in that portion of the meeting. The full body of scientific evidence, clinical trials and more than two decades of science and real world clinical experience continues to support the positive benefit/risk profile of Essure and its strong efficacy of 99.3% in patients who chose to rely on Essure for birth control.
****
Essure is an innovative Class III medical device that was approved under FDA's Premarket Approval (PMA) review, the agency's most rigorous pathway for medical devices. Since the initial application for Essure was approved in 2002, the agency has continued to review and approve Essure's safety and efficacy through 48 supplements to the original application.
On July 20, 2018, Bayer announced that it had made a business decision to voluntarily discontinue sales and distribution of the Essure System for Permanent Birth Control in the United States after December 31, 2018. This decision is based on a decline in U.S. sales of Essure in recent years and the conclusion that the Essure business is no longer sustainable. Several factors have contributed to declining interest in Essure among women in the U.S., including decreased use of permanent contraception overall, increased reliance on other birth control options, such as long-acting reversible contraceptives (LARCs), and inaccurate or misleading publicity about the device, such as The Bleeding Edge. Notably, the benefit-risk profile of Essure has not changed, and Bayer continues to stand behind the product's safety and efficacy.
About Essure
Essure is indicated for women who desire permanent birth control (female sterilization) by blocking the fallopian tubes.
Important Safety Information
WARNING: Some patients implanted with the Essure System for Permanent Birth Control have experienced and/or reported adverse events, including perforation of the uterus and/or fallopian tubes, identification of inserts in the abdominal or pelvic cavity, persistent pain, and suspected allergic or hypersensitivity reactions. If the device needs to be removed to address such an adverse event, a surgical procedure will be required. This information should be shared with patients considering sterilization with the Essure System of Permanent Birth Control during discussion of the benefits and risks of the device.
Essure is not right for you if you are uncertain about ending your fertility, suspect you are pregnant, can have only one insert placed, have had your tubes tied, have a known allergy to contrast dye, are unwilling to undergo the Essure Confirmation Test, have unexplained vaginal bleeding, or have suspected or known cancer of the female reproductive organs.
You should delay having the Essure procedure if you are or have been pregnant within the past 6 weeks, have an active gynecological infection, or are in the second half of your menstrual cycle.
Tell your doctor if you are taking immunosuppressants, have, or think that you may have, a history of metal allergies, or an allergy to polyester fibers, nickel, titanium, platinum, silver-tin, or stainless steel or any other components of the Essure system, are currently using an IUD for contraception, or have had or are considering a procedure to reduce bleeding from the uterus such as endometrial ablation.
WARNING: Be sure you are done having children before you undergo the Essure procedure. Essure is a permanent method of birth control.
WARNING: You must continue to use another form of birth control until you have your Essure Confirmation Test (3 months after the procedure) and your doctor tells you that you can rely on Essure for birth control. For some women, it may take longer than 3 months for Essure to be effective, requiring a repeat confirmation test at 6 months. Talk to your doctor about which method of birth control you should use during this period. If you rely on Essure for birth control before receiving confirmation from your doctor, you are at risk of getting pregnant.
During the Procedure: In the premarketing study, some women experienced mild to moderate pain (9.3%). Your doctor may be unable to place one or both Essure inserts correctly. In rare cases, part of an Essure insert may break off during placement. If breakage occurs, your doctor will remove the piece, if appropriate. There is a risk of perforation of the uterus or fallopian tube by the hysteroscope, Essure system or other instruments used during the procedure. In the original premarket studies, perforation due to the Essure insert occurred in 1.8% of women. A perforation may lead to bleeding or injury to bowel or bladder, which may require surgery. Your doctor may recommend a local anesthesia. Ask your doctor about the risks associated with this type of anesthesia.
Immediately Following the Procedure: In the premarketing study, some women experienced mild to moderate pain (12.9%) and/or cramping (29.6%), vaginal bleeding (6.8%), and pelvic or back discomfort for a few days. Some women experience headaches, nausea and/or vomiting (10.8%), or dizziness and/or fainting. You should arrange to have someone take you home after the procedure. In rare instances, an Essure insert may be expelled from the body.
During the Essure Confirmation Test: As one of the Essure Confirmation Tests (a modified HSG) requires an x-ray, you may be exposed to very low levels of radiation, as with most x-rays, if this test is used. Some women may experience nausea and/or vomiting, dizziness and/or fainting, cramping, pain or discomfort. In rare instances, women may experience spotting and/or infection.
Long-term Risks: Pain (acute or persistent) of varying intensity and length of time may occur and continue following Essure placement. This is also more likely to occur in women with a history of pain. There are reports of an Essure insert being located in the lower abdomen and pelvis. If this occurs, you cannot rely on Essure for birth control. Patients with known hypersensitivity to any of the components of the Essure system may experience an allergic reaction to the insert. In addition, some patients may develop an allergy to nickel or other components of the insert following placement. Symptoms reported in women using Essure that may be associated with an allergic reaction include hives, rash, swelling and itching. There is no reliable test to predict who may develop a reaction to the inserts. No birth control method is 100% effective. Ectopic pregnancies (pregnancy outside the uterus) may occur with Essure. This can be life-threatening. If insert removal is indicated, surgery will be necessary.
The safety and effectiveness of Essure has not been established in women under 21 or over 45 years old.
Essure does not protect against HIV or other sexually transmitted diseases.
Prescription Only
IMPORTANT
Caution: Federal law restricts this device to sale by or on the order of a physician. Device to be used only by physicians who are knowledgeable hysteroscopists; have read and understood the Instructions for Use and Physician Training Manual; and have successfully completed the Essure training program, including preceptoring in placement until competency is established, typically 5 cases.
The sale and distribution of this device are restricted to users and/or user facilities that provide information to patients about the risks and benefits of this device in the form and manner specified in the approved labeling provided by Bayer.
Talk to your doctor about Essure and whether it is right for you. Review the Patient-Doctor Discussion Checklist in the Patient Information Booklet with your doctor before deciding to have the Essure procedure.
About Bayer
Bayer is a global enterprise with core competencies in the Life Science fields of health care and agriculture. Its products and services are designed to benefit people and improve their quality of life. At the same time, the Group aims to create value through innovation, growth and high earning power. Bayer is committed to the principles of sustainable development and to its social and ethical responsibilities as a corporate citizen. In fiscal 2017, the Group employed around 99,800 people and had sales of EUR 35.0 billion. Capital expenditures amounted to EUR 2.4 billion, R&D expenses to EUR 4.5 billion. For more information, go to
# # #
© 2018 Bayer
Bayer and the Bayer Cross are registered trademarks of Bayer.
文章来源:
当医生往她们下体放虫子,是在放什么?
首发于公众号“影探”ID:ttyingtan
微博:影探探长
作者:钱老板
转载请注明出处
很多人都喜欢Netflix。
因为“网飞出品,必属精品”。
不过,相比它高质量的影视剧,我却更喜欢它耿直的纪录片。
这些片子往往带有强烈的自黑属性,喜欢揭露一些不为人知的社会问题。
前不久,网飞就又双叒叕拍了一部这样的纪录片,狠狠地批了一顿美国医疗器械的安全问题——
《尖端医疗的真相》
The Bleeding Edge

在美国,随着科技的迅猛发展,有一个行业的扩张速度夸张得有些吓人——医疗器械行业。
从一个人的出生到死亡,医疗器械帮助改善了无数人的生活质量,也拯救了许多生命。

据统计,过去十年,有超过7000万的美国人在体内植入了各式各样的医疗器械,比如心脏起搏器、白内障镜片、机械假肢...
可以说,很多人的一生都是伴随着各种医疗器械。
而很多医疗器械一旦被植入人体体内,往往也意味着它们将伴随患者一生。
比如妇女之友Essure。
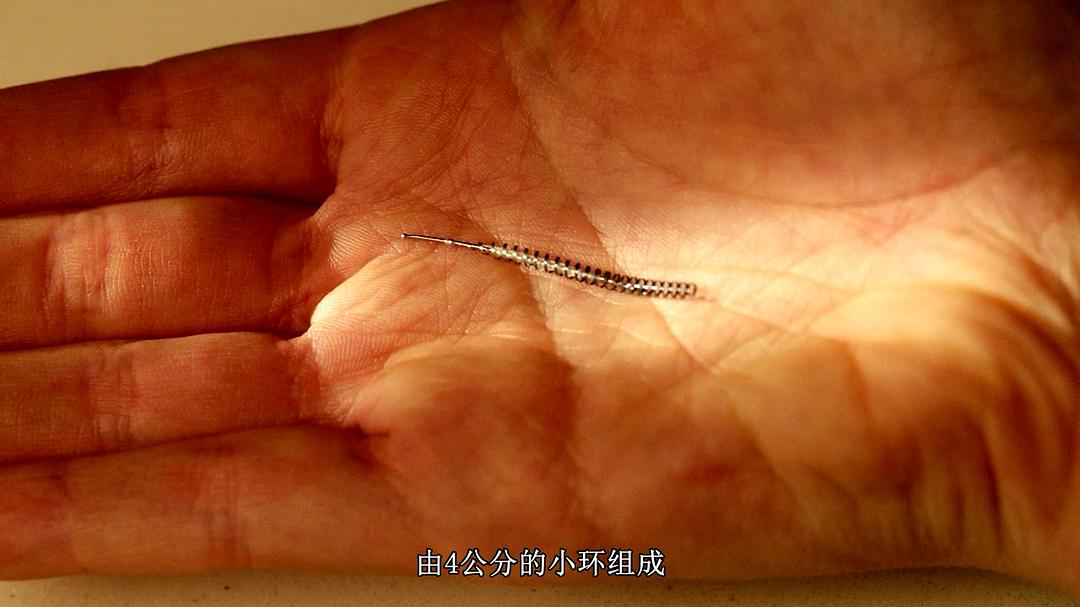
Essure是一款用于永久节育的医疗器械,于2002年获得美国FDA(Food and Drug Administration,食品药品监督管理局)批准使用,由医药行业巨头之一拜耳公司生产销售。
它的宣传语是:无需开刀,没有疤痕,永久有效,手术时间比你打两盘王者荣耀还短,99.9%的人用了都说好。
简直不要太诱人。

其原理也十分通俗易懂,即将Essure从子宫输入,放置于输卵管引起发炎反应,从而产生疤痕组织,达到永久封闭输卵管的效果。

听起来十分靠谱,对吧。
安吉尔一开始也是这么想的。

37岁的她原本是一个身体健康的邮递员,经过和丈夫商议,她决定去做绝育手术。
于是,妇产科的医生给她介绍了当时的最新尖端医疗科技Essure。
和广告上说的一样,手术很快就结束了。
但倒霉的是,安吉尔貌似中了奖,成了广告里说的那0.1%的人——她体内的植入的Essure发生了移位。
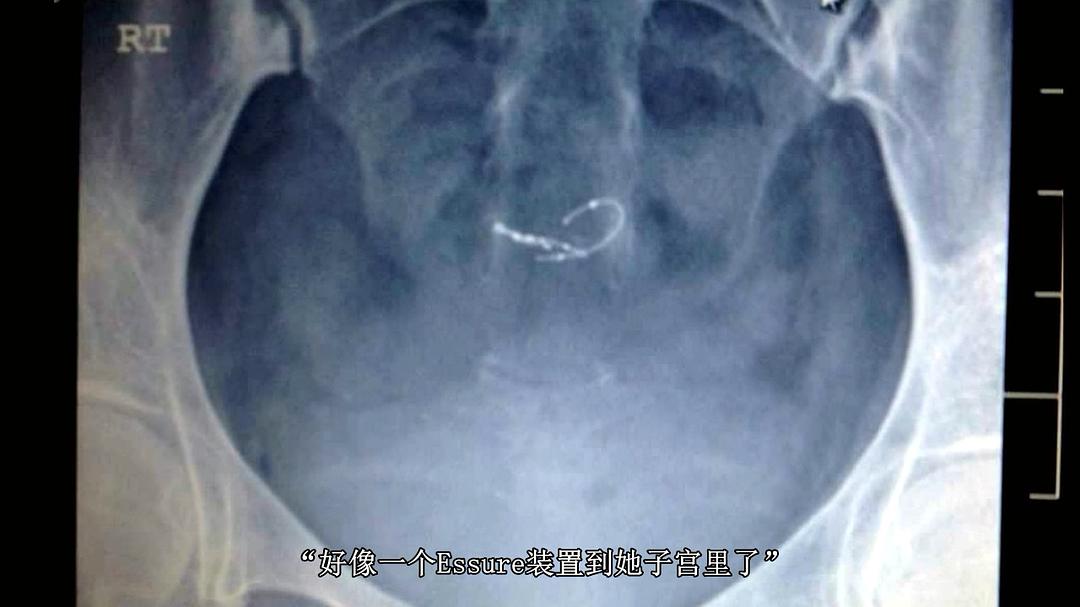
很快,她就出现了诸多不良反应。
不仅一个月二十几天都在出血,还经常高烧不退,常常伴有持续性刺痛感。
虽然后来通过手术取出了Essure,但只是取出了部分。
拜耳公司教会了医生们怎么植入,却没有教他们怎么取出,因为公司自己也不知道。
于是,医生们只好凭着感觉试图取出Essure,稍有不慎,器械就会破损,残留在患者体内。
而在现有医疗条件下,残屑是无法取出的。
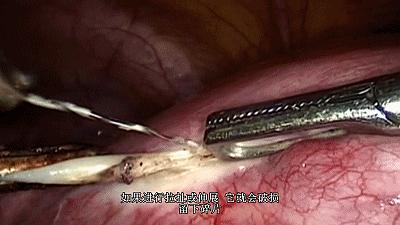
一旦发生这种情况,患者的余生可能都会受到影响,就像安吉尔。
她后来陆续又做了子宫切除手术、两次阴道修补手术以及三次关节手术。

护士听了都不敢相信
而一切的源头,都是来自于她体内残余的Essure碎片。
她不仅再也没法像正常母亲一样陪孩子们玩耍,也没法像正常女人一样和丈夫行床笫之欢。

这还算好的,至少她的丈夫对她依旧不离不弃。
安娜更惨。

她本来拥有一份正常工作,有四个女儿,家庭生活幸福美满。
植入Essure后,安娜同样出现了大出血,疼痛等问题,不得已,她做了Essure移除手术。
以前她从来不去医院,现在却成了医院的常客,因为她经常疼到昏过去。
她也因此丢了工作,丢了老公,不得不带着四个女儿在路边洗车过活。
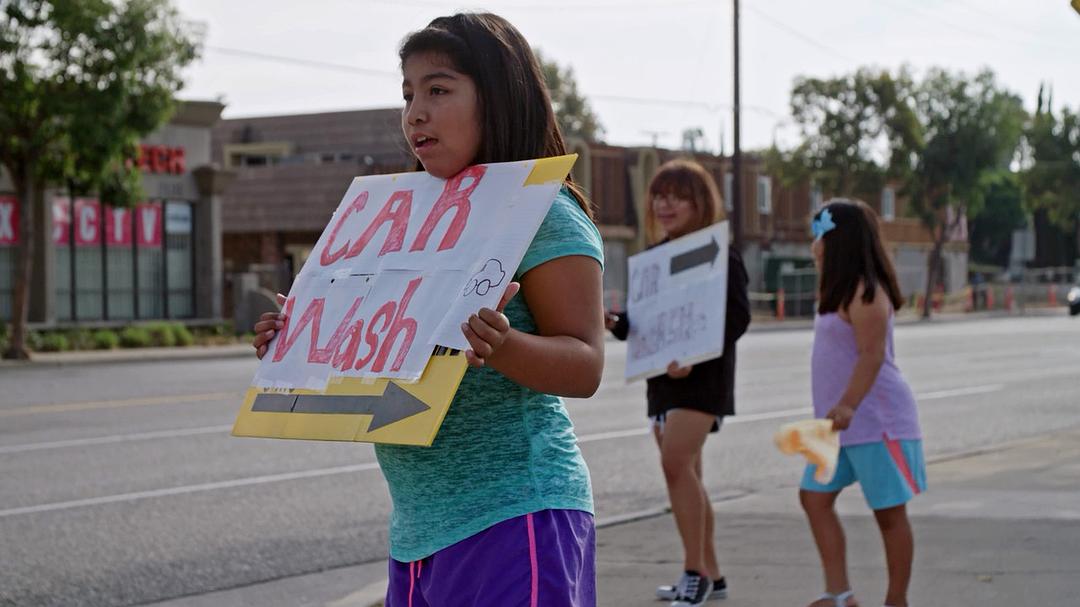
然而,拜耳公司对外宣称,这些人只是少数,网上能查到的有关Essure的负面消息也少得可怜。
甚至连安吉尔一开始也相信,自己只是太倒霉了。
直到她在facebook上建立了一个Essure问题小组。
她本想借此警告自己的亲戚朋友远离Essure,结果慢慢地竟然发展到了近4万成员。
她这才知道自己并非是那0.1%,也才真正开始了解到美国医疗器械行业背后的黑暗与肮脏。
在美国,大部分人都存在着一个思维误区:认为能投放到医院使用的医疗器械,一定经过了层层测试,安全有效。
但事实并非如此。
很多未经证实其安全性的医疗器械依然广泛地在市面上存在着。
比如,片中提到的另外三种医疗器械:网片、含钴假体、达芬奇机械手。
它们同样给不少病患带来了终生难以摆脱的疼痛和烦恼。


那么问题来了,这些存在缺陷的医疗器械是如何流通于市场的?
片中提到的原因其实涵盖了很多方面,但有三点相对来讲比较基础,也比较重要。
首先,监管制度陈旧。
都已经9102年了,但FDA(食品药品监督管理局)沿用的监管依据仍旧是颁布于1976年的《医疗器械修正案》。
这一法案,早已不适用于日新月异的医疗器械行业。

其次,关于医疗器械的审批制度存在着很严重的漏洞。
药物的审批流程十分严格,要经过两次临床试验,且必须有大量的病人样本。
可医药器械的审批就像是在过家家。
不仅只需要一次试验,而且研究规模往往很小,病人样本甚至可以少到只有50个。

在安吉尔调查的过程中,她弄到了2002年FDA审批Essure的会议视频记录。
里面的内容让人寒心。
在会议上,尽管有些科学家提出了可能发生的一些问题,各位达官贵人最终还是儿戏般地同意了Essure的审批。
他们在笑,笑科学家们是杞人忧天,笑说如果十年后发生了问题,那我们就得坐牢啦,哈哈哈。

且不说这些问题如今真的发生了,Essure植入人体关乎的是一个人一辈子健康的事情,他们为什么能笑着讨论,我真的不太懂。
FDA号称美国国民健康的守护者,各项药物、食品的标准至今仍走在世界前列。
但在医疗器械这方面,它像个笑话。

因为科技发展得太过迅速,医疗器械几乎每年都在更新,行业争辩说每次变动都做人体测试,成本太高。

于是国会设立了次于原有审批流程的510(K)流程:生产商只需要证明其器械基本等同于市面上已经存在的另一种器械即可。
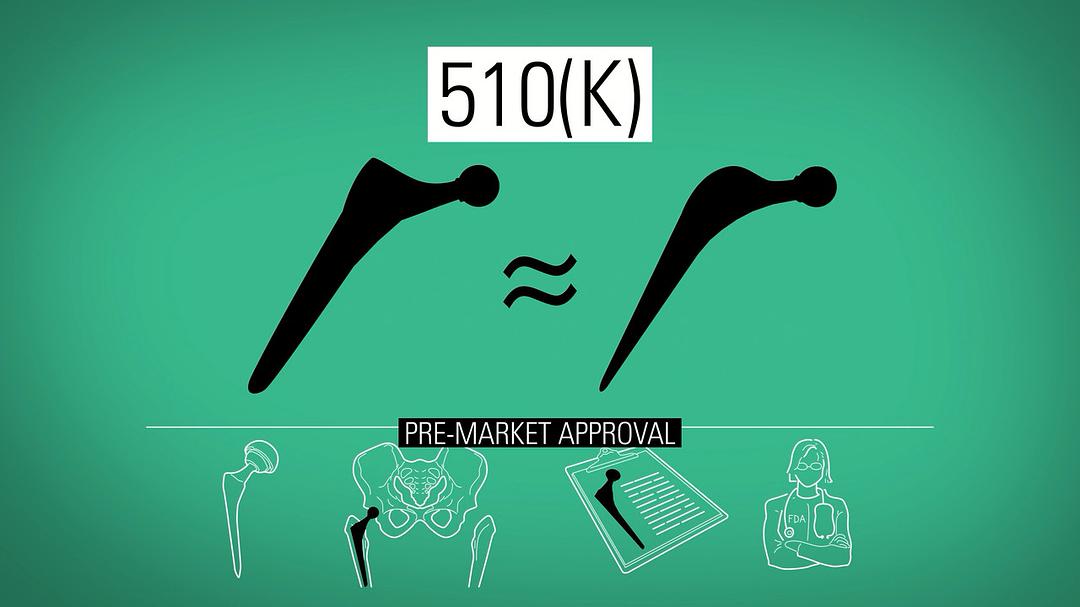
本来,这一规定是针对特殊情况。
却被各大医药公司钻了空子,硬生生把510(K)搞成了常态。
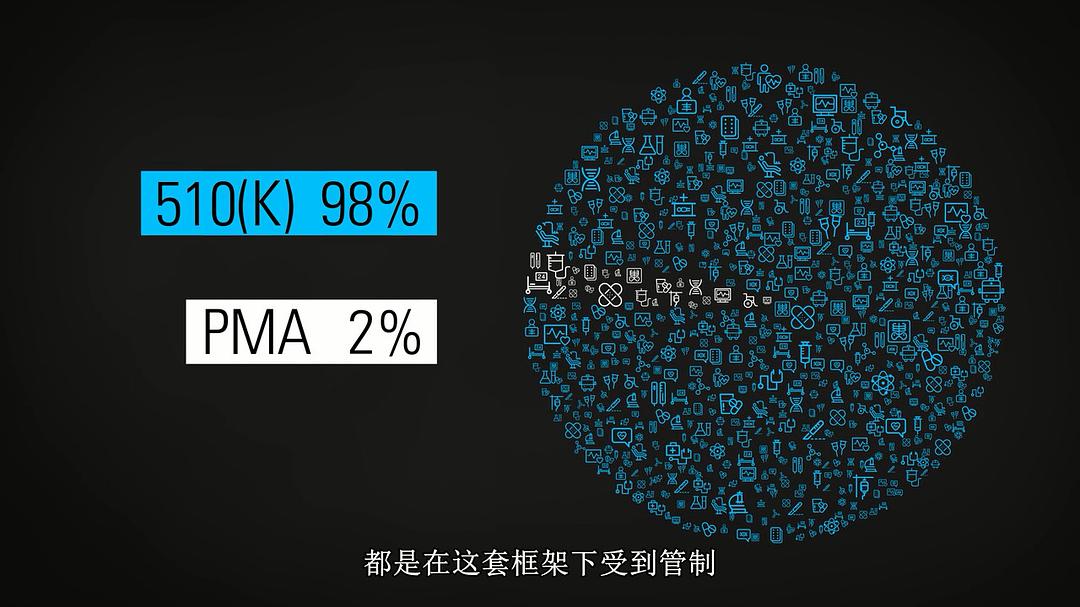
PMA:原有新药(器械)审查流程
而且,这一规定在本质上其实是个BUG。
一种器械获得审批的理由,是因为类似于前一种器械,但这前一种器械很有可能是类似于更早的一种器械,这成了一条循环链。
假如其中任何一款出现了问题,就意味着这一整个链条的器械都可能都有问题。

比如纪录片中的讲到的另一款医疗器械——钴铬合金髋关节假体。
正是因为它依葫芦画瓢,照着以前塑料或者陶瓷材料的假体制作,才通过了510(K)的审批。

但厂商们不知道的是,长期佩戴此类假体会导致病人体内的钴浓度严重超标,进而影响到病人的认知功能。
大部分的病人,还以为自己得的是无法根治的老年痴呆症。
但实际上,他们只需要换一副假体就好了。

虽然生产厂商召回了一些含钴假体,打的却是“因其会引起周边组织破损”的旗号。
不仅如此,医疗器械行业仍然推荐医生和病人使用含钴假体,至今,全世界仍有1000多万的人植入了含钴假体。
厂家们的意思我大概能明白,应该是想趁还未大面积曝光,能卖多少是多少。

而这一现象,也在一定程度上解释了为什么会出现这么多医疗器械事故的根本原因。
说到底,还是庞大资本的推动和巨大利益的驱使。
医疗器械这块蛋糕有多大?
在《福布斯》杂志的一篇报道中有分析表明,到2022年,医疗器械产业的规模将达到5300亿。
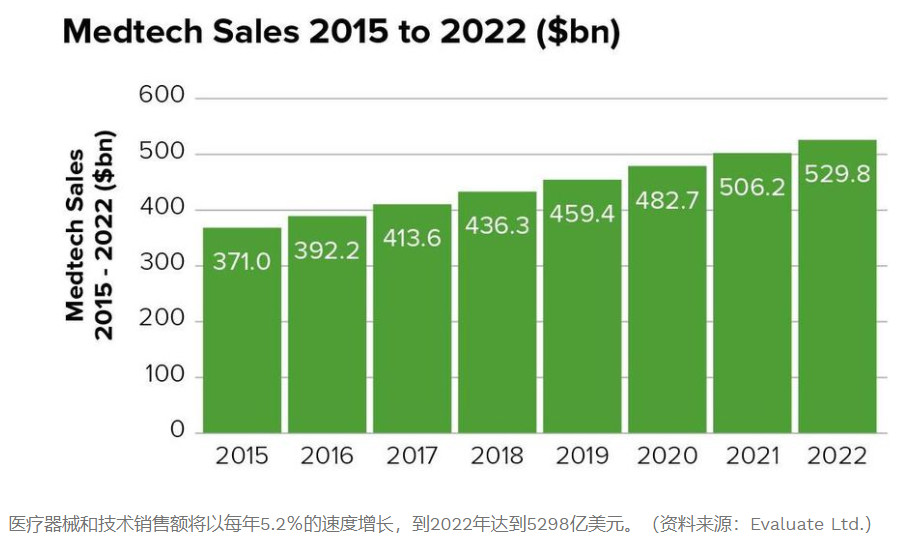
5300亿什么概念?
如果按100美元来算,这些钱连起来可以绕地球20多圈。
在片中,医疗器械公司生产的一款植入式网片,上市成本25美元,售价2000美元。
虽然片中没有提到研发成本这一项,但从此前的种种迹象来看,研发阶段很可能也注了不少水,能省则省。
而庞大利润所影响的,是自上而下整个行业链。

政客、FDA、医院,一一疏通。
往上了说,绝大多数FDA的官员本身就来自于医疗器械行业,卸任后又回归到各大医疗器械公司,协助他们规避监管。



在2014年美国国会联合工作人员的报告中,有人调查到FDA曾购买监控软件,用以报复秘密检举的人。
两秒钟截屏,键盘按键记录,亦或是直接找借口开除,由不得你不怕。

往下了说,大部分医生实际上没有时间和精力去查证那些器材是否危险,那不是他们的专业领域。
他们能倚靠和相信的,也只有FDA和医疗器械公司给出的数据。
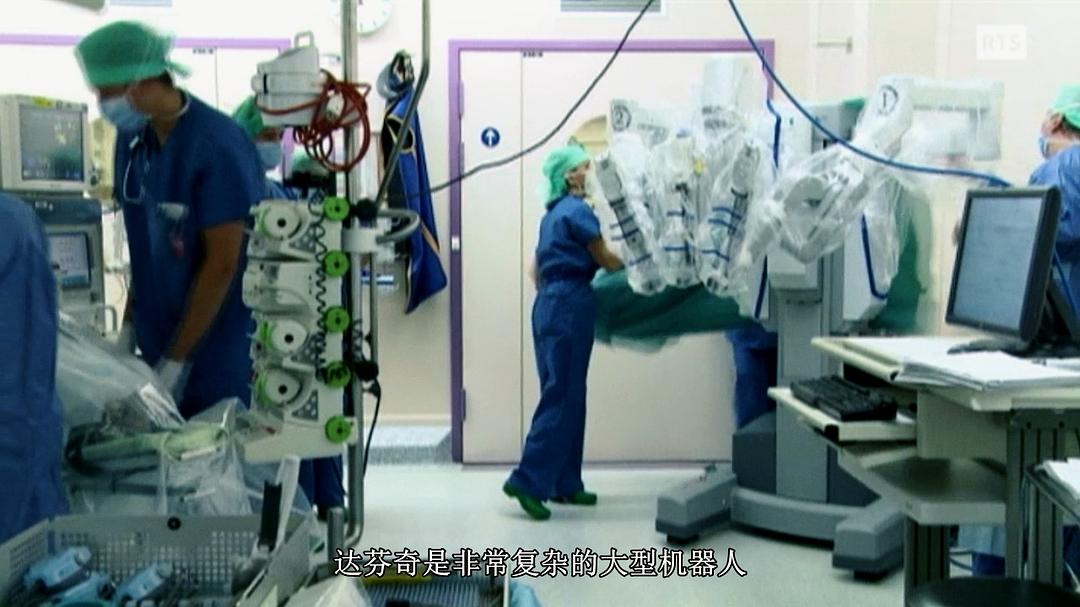
他们会真的以为,操作一台新上市的手术机器人,只需要十场手术经验。
而真相是,如果医疗器械公司如实告诉医院“医生们需要进行九个星期的培训才能熟练掌握”,那么,就根本不会有人愿意买。

更何况,有些医生目的很明确,就是为了拿分红才拼命帮医疗器械公司推销产品。
在美国,很多回扣甚至是合法的。
即便是不合法,那也保不准医疗器械公司会赞助医生开个会、出个国、洗个脚、唱个歌什么的是不是。
再比如,我觉得这个医疗器械科主任的儿子好可爱,我好喜欢,我要出10万块给他买一只镶钻钢笔,帮助他好好学习,长大了好为美国做贡献。
送钱的理由简直感天动地,无懈可击。

最后受苦的,还是老百姓。
他们能懂什么呢,小时候“听老师的”,长大了“听医生的”。

好在,还有安吉尔这样敢于为自身权利发声的人,她们去妇科国际会议门口游行,她们去找议员给国会施压。
她们暂时是胜利了。
目前,拜耳公司在欧洲和美国都撤下了所有在售的Essure。
但公司仍不承认产品存在安全问题,坚称是出于商业上的考虑。
而且在片中,也没有任何一位FDA和医疗器械公司的成员愿意接受出境采访。

网飞和导演都很清楚,这条路还很长。
他们也只能在片尾告诉观众,好好照顾自己。

片尾的安全忠告
但至少现在你看到了,我也看到了。
那么,这条抗争之路就应该算是又前进了一步吧。
版权归作者所有,任何形式转载请联系作者。
文/钱老板
(更多原创影评,微信搜索ttyingtan,后台回复片名,一起来看片儿~)


